Атом је најмања јединица елемента која задржава његова хемијска својства. Он je темељ материје: све око нас – од ваздуха и воде, до стена, биљака и животиња, као и све унутар наших тела, сачињено је од атома.
Иако су антички Грци веровали да су атоми најмање честице које постоје (сама реч „атом“ потиче од грчке речи за „недељиво“), они су далеко мањи него што можемо да замислимо.

Да би сте стекли представу о њиховој величини замислите влас људске косе, дебеле колико и 500.000 атома угљеника наслаганих један на други.
Атоми се не могу видети голим оком нити стандардним микроскопом јер су сувише мали да би скренули таласе видљиве светлости. Могу се посматрати само помоћу електронских микроскопа или посебних ласерских метода које подстичу атоме да емитују светлост.
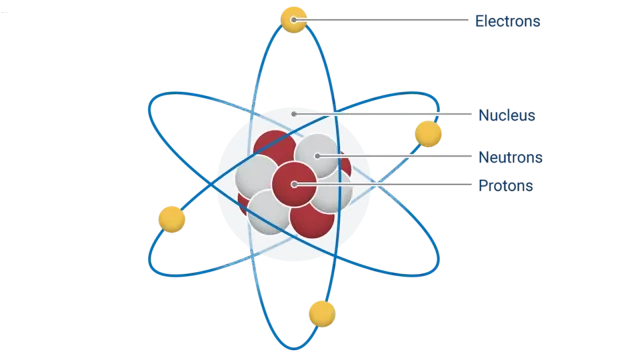
Сваки атом се састоји од три главна типа честица:
- Протони су позитивно наелектрисане честице. Број протона у језгру одређује о ком елементу је реч (нпр. један протон је водоник, док је осам протона – кисеоник).
- Неутрони су неутралне честице које се налазе у језгру.
- Електрони су негативно наелектрисане честице које окружују језгро у облику облака.
Језгро (нуклеус) се налази у центру атома и садржи протоне и неутроне. Оно је невероватно густо и мало у поређењу са целим атомом – ако би језгро било величине кликера, атом би био величине спортског стадиона. Језгро на окупу држи „нуклеарна сила“ која је на малим растојањима далеко јача од електричног одбијања између позитивних протона.

Атоми су обично неутрални јер имају једнак број протона и електрона. Међутим, промене у овом балансу доводе до занимљивих појава:
- Ако атом добије или изгуби електроне, он постаје јон. Јонизовани атоми имају јако електрично поље и снажно привлаче супротно наелектрисане честице.
- Излагање гама или рендгенском зрачењу може отргнути електроне из атома, што може хемијски изменити материјале или оштетити ДНК у живим ткивима.
- Код нестабилних атома, језгро не може да задржи све честице на окупу. Тада се атом „распада“ и ослобађа енергију у облику зрачења (алфа и бета честице, гама зраци).
Године 1917, Ернест Радерфорд (Ernest Rutherford) је открио да се испаљивањем алфа честица у азот овај елемент може претворити у кисеоник, при чему се избацује језгро водоника — касније названо протон.
Ово је довело до развоја акцелератора честица. Ове моћне машине убрзавају честице скоро до брзине светлости како би „разбиле“ атоме. Данас се акцелератори користе за стварање радиоактивних материјала у медицини (нпр. за лечење канцера), стерилизацију медицинске опреме, истраживања порекла универзума која се спроводе у CERN-у (Conseil européen pour la recherche nucléaire), као и анализу ваздуха и унапређење материјала.
Нуклеарна фисија
Током 1930-их откривено је да испаљивање неутрона у одређене атоме уранијума изазива њихово цепање на два дела — процес назван фисија.
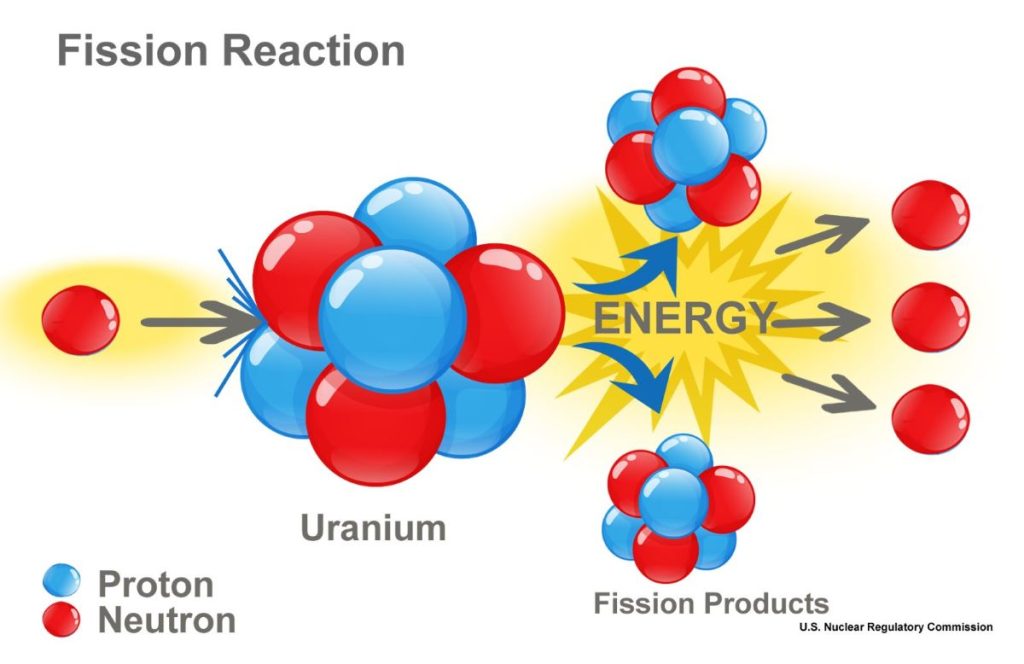
- При сваком цепању ослобађа се просечно 2,5 неутрона који даље цепају друга језгра. Ово је процес ланчане реакције.
- Да би фисија била ефикасна, користе се вода или графит како би се успорили „брзи“ неутрони.
- Фисија се данас користи за производњу чисте енергије, што чини 10% светске енергије без емисије угљен-диоксида.
Нуклеарна фузија
За разлику од фисије, фузија је процес спајања два лака атомска језгра у једно теже.
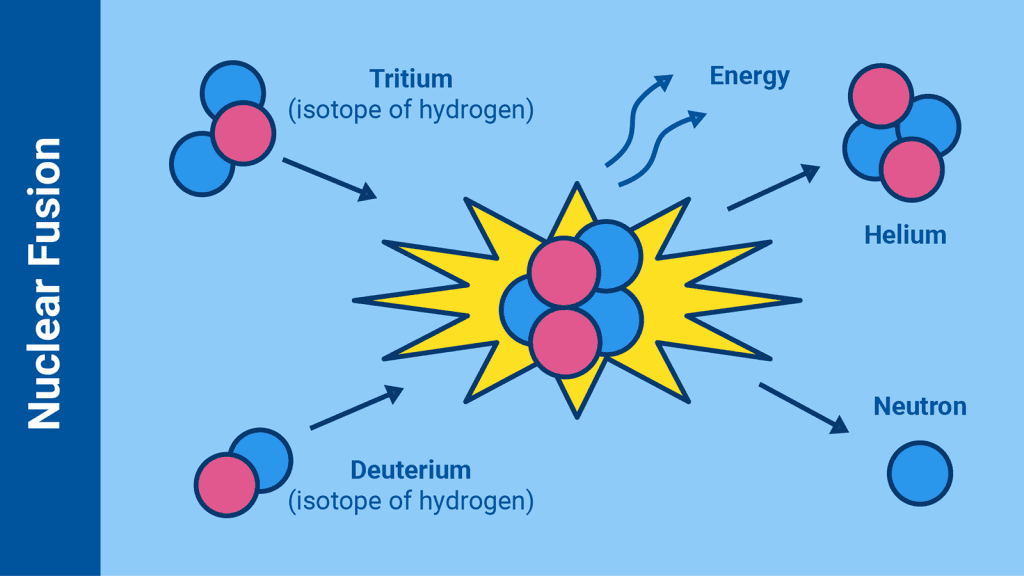
- Овај процес се одвија у стању плазме — врелом гасу сачињеном од јона и слободних електрона.
- Да би се савладало електрично одбијање и створили услови за фузију, потребне су температуре од око 100 милиона степени Целзијуса.
- Сунце производи енергију управо овом реакцијом, захваљујући својој огромној гравитацији и притиску који омогућавају језгрима да се споје.